Capacités sensitives de la cellule aux forces mécaniques

inspiré de La Création d’Adam par Michel-Ange, 1512, Chapelle Sixtine
Revue bibliographique 2019
revue bibliographique réalisée en 2019 pour l’UE Scientific Communications dans le cadre de l’obtention du Master 2 Biologie Moléculaire et Cellulaire, parcours Génétique et Biologie de le Cellule et Pathologies.
Cette revue fait écho à l’actualité, le Prix Nobel 2021 de Physiologie ayant été attribué à David Julius et Ardem Patapoutian pour leurs travaux sur le toucher via les protéines Piezo et TRPV
édité le 30 mars 2022
Résumé
Le mécanosensing correspond à la détection du signal mécanique permettant sa transformation en signal électrochimique. Les contraintes de compression activent des voies de signalisation différentes de celles des contraintes d’étirement, mais ces deux types sont souvent confondus dans la littérature. Dans cette revue, les données actuelles seront présentées permettant un éclairage neuf sur les différents mécanismes liés à la détection du signal mécanique lors des forces de compression (qui surviennent notamment lors du toucher).
Introduction
La transformation du signal mécanique en signal électrochimique _ou mécanotransduction_ est indispensable à de nombreux phénomènes cellulaires tels que la croissance osseuse ou encore la transformation des cellules souches. [1] L’impact de la compression sur les voies moléculaires est principalement lié à l’ouverture des canaux ioniques.
Mais à l’inverse des forces d’étirement, le mécanisme permettant la détection du signal _ou mecanosensing _ de compression reste peu connu et les précédentes revues sur le sujet restent très incomplètes face aux données actuelles. [2] Dans les cellules souches mésenchymateuses par exemple, la transduction du signal est liée aux ions calcium qui vont réguler certains processus par l’association de ces ions à différentes protéines régulatrices comme la Calmoduline, la Troponine C, l’Annexine ou la Calpaine. [2] Les principales causes de ‘investigation des processus est que la transmission du signal est multimodale et de nombreux biais technologiques restreignent la caractérisation spécifique de chaque voie empruntée, entrainant ainsi une confusion entre compression et étirement. Aussi, elle est souvent mélangée avec d’autres types de sollicitations mécaniques Contrairement à l’étirement, le mécanosensing de la compression est souvent détectée indirectement, lié à l’augmentation de la pression hydrostatique du liquide compris entre l’origine de la compression et la cellule.
Le but de cette étude est de mettre à jour les connaissances sur les mécanismes de détection des contraintes de compression stricte conduisant à la transmission d’un signal.
La compression au niveau de la membrane cellulaire
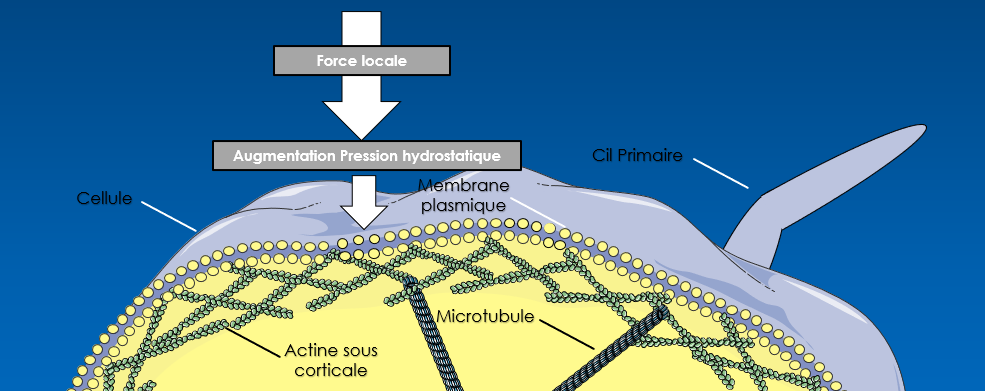
In vivo, la compression impacte la cellule dans son ensemble. La membrane va se déformer, modifiant la taille et la conformation de la cellule afin de résister à la contrainte qui lui est imposée, affectant le cytosquelette à deux niveaux. D’une part, le réseau de microtubules va se déformer grâce à la repolarisation des microtubules permettant leur déformabilité, puis les microtubules vont s’acétyler afin de résister aux contraintes mécaniques. Cette acétylation a été prouvée dans différents modèles, mais un papier récent a montré le lien entre cette acétylation et l’ouverture des canaux ioniques chez la drosophile. En effet, la mise en tension des microtubules va favoriser le changement de conformation du canal membranaire Trpv1 _ que l’on retrouve également chez les mammifères_ favorisant l’entrée de Ca2+. [3] [Figure 1c]
D’autre part, le cortex d’actine sous-membranaire permet de répartir les forces sur l’ensemble du cytosquelette. Les fibres d’actine vont s’étirer modifiant la conformation de protéines des canaux membranaires tels que Trpv4, permettant une entrée non spécifique de Ca2+. L’augmentation de calcium intracellulaire va stimuler les récepteurs calciques RhoA qui vont permettre la contraction de la myosine du cortex d’actine. [4] L’augmentation de rigidité induite favorise la régulation de cet apport calcique par RhoA et modifie la localisation dans les fibroblastes humains du mécanosenseur Yap. [Figure 1a] Classiquement dans le noyau, la compression entraine la sortie de la protéine dans le cytoplasme activant les différentes voies de signalisation associées aux Yap/Taz. [2] Dans le même temps, l’activation de RhoA par le calcium va augmenter la stabilité des microtubules entretenant davantage l’ouverture des canaux calciques non spécifiques comme Trpv1. [3]
Piezo, le mécanosensing spécifique
Il existe différents canaux ioniques impliqués dans le mécanosensing au niveau de la membrane cellulaire, tels que les protéines Kcnk2, MscS ou Trpv4. Néanmoins, seulement celles permettant le passage des ions calcium ont été décrites comme liées à la compression. [5] L’emploi du microscope à force atomique (AFM) a permis l’activation spécifique de Piezo dans les chondrocytes par l’application d’une augmentation locale des forces compressives sur la membrane cellulaire. [1] Lors d’une augmentation de la pression hydrostatique, cette protéine permet sous sa forme dimérisée le passage d’ions calcium à travers la membrane et est retrouvée sous deux isoformes Piezo2 et Piezo1. Cette forme est celle retrouvée dans le plus de types cellulaires humains différents et est sensible au passage du calcium. C’est cette sensibilité aux cations qui permet la transmission du signal mécanique car elle régule l’ouverture du canal créant une polarisation très limitée dans le temps et dans l’espace. Malgré l’augmentation de la pression hydrostatique extérieure, le canal ne se rouvrira pas tant que la polarité initiale ne sera pas complètement rétablie créant une mécanotransduction très précise. [5] De plus, la conformation des sous unités de la protéine permet l’ouverture du canal de différentes manières, mais l’impact sur le passage du Ca2+ et donc sur une possible modulation du signal transduit n’a pas été mesurée.
Le cil primaire
Le cil primaire est une structure fusiforme composé d’un assemblage de microtubules rattaché à la cellule via un centriole. Orienté dans la partie apicale des cellules polarisées il est impliqué dans les principales voies de signalisation grâce à sa capacité à ressentir son environnement. [6] Le mécanosensing dans cette conformation rejoint celle décrite dans les cellules souches mésenchymateuses puisque c’est l’entrée de calcium via les canaux Trpv4 qui va être à l’origine de la transduction du signal de compression. La protéine Trpv4 s’ouvre par étirement de la membrane, la déformation du cil primaire favorise l’ouverture du canal ionique. [3] [Figure 1d] Trpv4 est associé dans le cil primaire du rein à la protéine Trpp2 qui est également un canal ionique, perméable au Ca2+ comme l’on pouvait s’y attendre, mais aussi au K+ ouvrant la voie à d’autres potentiel types de mécanosensing en absence de matrice extracellulaire. [7]
La compression est à l’origine de la modification de l’orientation et de la tension des composants de la matrice extracellulaire. Elle entraine l’activation de nombreuses voies de signalisation liées à l’interaction du cil avec son microenvironnement. [6] Mais la mécanotransduction induite n’est pas spécifique à celle de la compression et reflète la signalisation induite lors des contraintes d’étirement.
Conclusion
Les protéines formant les canaux ioniques en particulier pour le passage du Ca2+ et leur ouverture sous l’influence d’une augmentation de la pression hydrostatique sont les éléments les plus impliquées dans la transmission du signal mécanique lors des contraintes de compression. Piezo semble être le canal le plus spécifique du mécanosensing jouant un rôle lors de la compression dans la voie MAPK, ERK et JNK notamment. [2] Néanmoins, les canaux ioniques non spécifiques possèdent une régulation fine liée à la déformabilité des protéines en fonction de l’intensité des forces compressives. [8] En effet, une compression trop intense ou au contraire pas assez ne permettra pas aux canaux ioniques de permettre l’entrée du Ca2+ donc de la mécanotransduction.
Dans le cas du cancer du sein, les acini des cellules épithéliales sont remplis de composés de la matrice extracellulaire à cause d’une sécrétion anarchique des CAF (Cancer Associated Fibroblasts). Cet envahissement luminal modifie la structure des cellules et modifie la résistance globale mais aussi intrinsèque de chaque cellule épithéliale. La modification du sensing dû au changement de l’environnement cellulaire modifie et le comportement cellulaire et ses propriétés de résistance face aux contraintes de compression. [9] Effectivement, on observe une diminution de la présence du cil primaire dans les cancers du sein. La régression du cil primaire par la cellule épithéliale traduit un comportement adaptatif et deux hypothèses sont retenues. La première souligne un comportement de préservation car les signaux du microenvironnement sur le cil libre stimulent la voie Hedgehog et favorise le développement tumoral. La deuxième hypothèse met en exergue l’importance de la signalisation calcique qu’induit Trpv4. Le développement anarchique dans la lumière de l’acini risque d’augmenter la pression hydrostatique au contact du cil et d’enclencher les voies de signalisation illustrant bien l’importance du mécanosensing dans le développement tumoral. [10] Notre revue permet de développer cette conclusion et de différencier le fonctionnement de Trpv4 membranaire de celui de Trpv4 ciliaire, ouvrant la voie à un futur axe de recherche.
Références
[1] Sugimoto, A. et al. Piezo type mechanosensitive ion channel component 1 functions as a regulator of the cell fate determination of mesenchymal stem cells. Sci Rep 7, 17696 (2017).
[2] Liu, Y.-S. & Lee, O. K. In Search of the Pivot Point of Mechanotransduction: Mechanosensing of Stem Cells. Cell Transplant. 23, 1–11 (2014).
[3] Yan, C. et al. Microtubule Acetylation Is Required for Mechanosensation in Drosophila. Cell Rep 25, 1051-1065.e6 (2018).
[4] He, L. et al. Role of membrane-tension gated Ca2+ flux in cell mechanosensation. J Cell Sci 131, jcs208470 (2018).
[5] Wu, J., Lewis, A. H. & Grandl, J. Touch, Tension, and Transduction – The Function and Regulation of Piezo Ion Channels. Trends in Biochemical Sciences 42, 57–71 (2017).
[6] Seeger-Nukpezah, T. & Golemis, E. A. The extracellular matrix and ciliary signaling. Curr Opin Cell Biol 24, 652–661 (2012).
[7] Köttgen, M. et al. TRPP2 and TRPV4 form a polymodal sensory channel complex. J. Cell Biol. 182, 437–447 (2008).
[8] Sabass, B. & Stone, H. A. Role of the Membrane for Mechanosensing by Tethered Channels. Phys. Rev. Lett. 116, 258101 (2016).
[9] Venugopalan, G. et al. Multicellular Architecture of Malignant Breast Epithelia Influences Mechanics. PLoS One 9, e101955 (2014).
[10] Yuan, K. et al. Primary cilia are decreased in breast cancer: analysis of a collection of human breast cancer cell lines and tissues. J. Histochem. Cytochem. 58, 857–870 (2010).
